Novo medicamento para tratar DMRI
O FDA, órgão do governo dos EUA responsável para autorização de novos medicamentos, aprovou um novo tratamento para DMRI úmida. A partir do ano de 2020, a injeção de Brolucizumabe vai estar disponível para uso nos pacientes. A previsão é de estar disponível no Brasil a partir de abril de 2020.
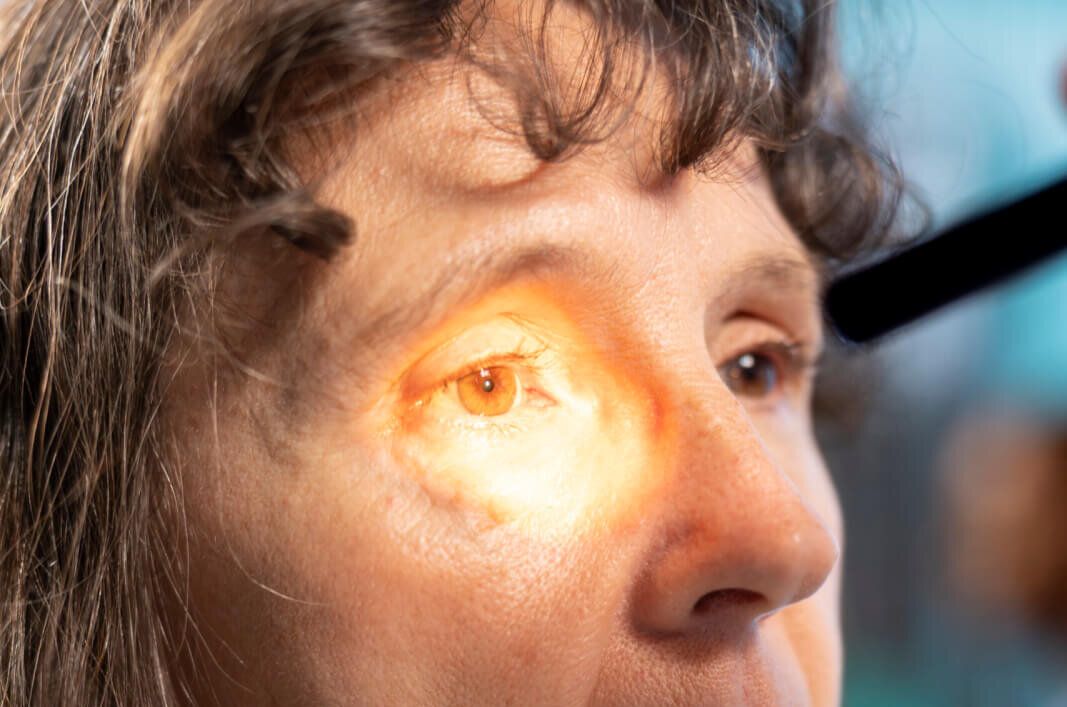
A DMRI úmida é a principal causa de cegueira em idosos. É um distúrbio ocular degenerativo crônico no qual um excesso de proteína VEGF faz com que os vasos sanguíneos anormais cresçam sob a retina e a mácula, causando vazamento de líquido. Isso distorce a visão central e, eventualmente, causa cegueira.
O Brolucizumabe fornece uma alta concentração de moléculas anti-VEGF e vem somar a outras opções já disponíveis, como Aflibercept e Ranibizumabe. A diferença entre eles é na frequência de injeções, que poderá ser espaçada e os pacientes podem ser tratados a cada 3 meses. Com isso, o paciente fica mais tempo coberto pelo tratamento e com menos necessidade de se submeter às injeções.
O Brolucizumabe, também conhecido como RTH258, pode ser administrado a pacientes elegíveis com DMRI úmida a cada 3 meses, imediatamente após uma fase de carregamento de 3 meses.
A aprovação segue a consideração dos dados de dois ensaios de fase III, HAWK e HARRIER. O Brolucizumabe não se mostrou inferior à injeção de Aflibercept (Eylea) no intervalo de 1 ano do estudo.
Assim que disponível no Brasil, a Viver oftalmologia terá acesso e iniciará o uso para pacientes indicados. Continue acompanhando e manteremos informados.